Учеба и наука
Решено
Реакции выражаются схемами: MnSO4 + KClO3 + KOH = K2MnO4 + KCl + K2SO4 + H2O; Ni(NO3)2 = NiO + NO2 + O2. Составьте электронные уравнения, расставьте... - вопрос №1004925
коэффициенты, определите окислитель и восстановитель в каждой реакции. К какому типу относится каждая из приведенных реакций?
март 27, 2014 г.
-
Всего ответов: 2
-
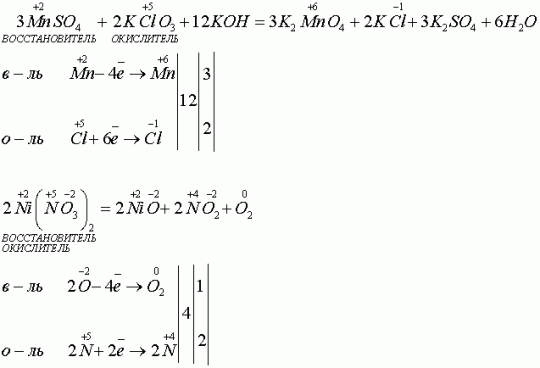 Лучший ответ по мнению автора
Лучший ответ по мнению автора -
МnSO4 + KClO3 + KOH ®K2MnO4 + KCl + K2SO4 + H2O– схема реакции
Электронно-ионный баланс:
Мn2+ 8OH- — 6e®MnO42- + 4H2O 1 – восстановитель, окисление
ClO3- + 3H2O + 6e®Cl- + 6OH- 1 – окислитель, восстановление
Мn2+ 2OH- + ClO3-®MnO42- + H2O + Cl- – ионное уравнение
МnSO4 + KClO3 + 2KOH®K2MnO4 + KCl + K2SO4 + H2O – молекулярное уравнение. Это межмолекулярная ОВР.
Ni(NO3)2 ®NiO + NO2 + O2 – схемареакции
Электронный баланс:
N+5 + 1e®N+4 4 – окислитель, восстановление
2O-2 — 4 e®O20 1– восстановитель, окисление
2Ni2+ + 4NO3- ® 2NiO + 4NO2 + O2 – ионное уравнение
2Ni(NO3)2 ®2NiO + 4NO2 + O2 – молекулярное уравнение. Это внутримолекулярная ОВР, окислитель и восстановитель находятся в одной частице вещества.
Похожие вопросы
Для силиката магния, иодоводородной кислоты построить графические формулы и указать виды химической связи в молекулах на основании значений электроотрицательности атомов.
апрель 17, 2024 г.
Решено
Рассчитайте объем (м^3) (при н.у) кислорода необходимый для полного сгорания 3,96кг кокса , содержащего 10% примесей . ответ ОКРУГЛИТЕ ДО СОТЫХ ДОЛЕЙ ЕДИНИЦЫ
апрель 15, 2024 г.


