Учеба и наука
Смешали два раствора, содержащих соответственно 33,3 г хлорида кальция и 16,4 г фосфата натрия. Вычислите массу образовавшегося фосфата кальция. - вопрос №3477889
октябрь 16, 2019 г.
-
Всего ответов: 2
-
2Na3PO4 + 3CaCl2 = Ca3(PO4)2 + 6NaCl
n(Na3PO4) = 16.4(г)/164(г/моль) = 0,1 моль
n(CaCl2) = 33.3(г)/111 (г/моль) = 0,3 моль
на 2 моль Na3PO4 приходится 3 моль CaCl2
на 0,1 моль -//- х моль
х = 0,1*0,3/2 = 0,15 моль
CaCl2 - в избытке
на 2 моль Na3PO4 приходится 1 моль Ca3(PO4)2
на 0,1 моль -//- х моль
х= 0,1*1/2 = 0,05 моль
m (Ca3(PO4)2) = nM = 0.05 моль*310г/моль = 15,5 г -
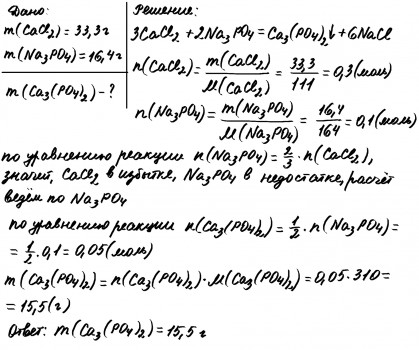
Похожие вопросы
Постройте график функции y=x^2-2x-8. Найдите с помощью графика : a)Значение y при x = -1,5; б) Значение х при которых у=3; в) Нули функции;промежутки в которых у>0 и в которых у<0; г)
октябрь 24, 2017 г.
Как получить 49 из этих цифр? Нужен алгоритм. Цифры: +2 +3 +5 *2 *3 *5 Если выбрал какую то цифру, то повторять ее нельзя
октябрь 14, 2019 г.
Вычислить площадь треугольника с вершинами А(7;3;4), В(1;0;6), С(4;5;-2)
октябрь 6, 2017 г.


